
2026年4月21日,由河南省医疗器械商会主办的“一带一路共建国家医疗器械出海及UDI合规实施公益培训班”,在郑州安图生物产业园成功举办。
本次培训是河南省医疗器械行业响应国家“一带一路”高质量发展倡议、服务企业国际化战略的重要举措,旨在深入贯彻国家药监局对医疗器械唯一标识(UDI)及文件管理的最新法规要求。
培训汇聚了来自各地医疗器械生产、经营企业的法规事务负责人、质量负责人、国际注册专员等近百位行业骨干,课程紧扣政策前沿与企业实务,堪称一次高规格、强落地的行业知识盛会。


作为本次培训的联合举办单位与核心技术支持方,睿展数据受邀出席,并围绕新版《医疗器械生产质量管理规范》下的UDI实施与体系文件管理,为参会企业带来了两场深度培训分享,获得现场热烈反响。
01 / 政策紧迫:新版GMP下,UDI与DMS已成“必选项”
2025年11月4日,国家药品监督管理局正式颁布新版《医疗器械生产质量管理规范》(2025年第107号),并明确该规范自2026年11月1日起正式施行。这意味着,距离新版GMP全面落地仅剩不到7个月,合规的倒计时已经开启。
新规对UDI和体系文件管理提出了远高于旧版的要求:
UDI:企业须建立UDI实施程序,确保产品可追溯。未合规将面临上市受阻、飞检重点核查等风险。
DMS:新规强化文件控制与记录管理,传统模式难以满足实时受控、版本追溯要求。文件管理混乱可直接导致停产整改。
目前,各地药监已开始依据新版要求进行模拟检查或预审指导,过渡期正在快速收窄。合规是生存题——能否在2026年11月1日前快速落地UDI与数字化文件管理体系,直接决定了企业能否顺利取得或维持生产许可,守住市场准入资格。
02 / 聚焦两大核心议题,干货培训赋能企业
在培训现场,睿展数据产品总监、UDI首席讲师林磊,结合新版《医疗器械生产质量管理规范》的最新要求,针对企业在实际落地中的痛点,分别作了两个主题分享:
一、《基于新版GMP的UDI实施指导与经验分享》
系统梳理了从发码、编码赋码到上报公示的全流程实施路径,结合多个成功案例,详细解析了企业如何低成本、高效率地搭建合规、可追溯的UDI管理体系。
二、《基于新版GMP的体系文件管理法规解读与数智化解决方案》
深入解读了新规对文件管理、记录控制等条款的更新要求,并展示了睿展数据DMS(体系文件管理系统) 如何帮助企业实现体系文件的数字化、流程化、合规化管控,有效应对现场检查。
分享结束后,林磊老师与参会企业代表进行了面对面答疑,针对UDI实施中的标签设计、数据库对接、文件版本控制等实际问题提供了切实可行的建议。


03 / 睿展数据:合规+数智化,UDI+DMS真正落地
新版GMP实施在即,企业面临两大核心课题:UDI如何实现合规落地?体系文件管理怎样满足电子记录与可追溯要求?睿展数据的解决方案正是精准应对这些挑战而生。
睿展数据是国家高新技术企业,并通过了CMMI5国际认证,长期深耕医疗器械数字化领域,是国内屈指可数的能够提供“合规+数智化”一体化解决方案的头部服务商。依托自主研发的技术平台与专业的服务团队,公司服务网络已覆盖全国20多个省份,累计服务客户上万家,已为众多企业提供了既贴合法规要求、又可长期稳定运行的合规支持。
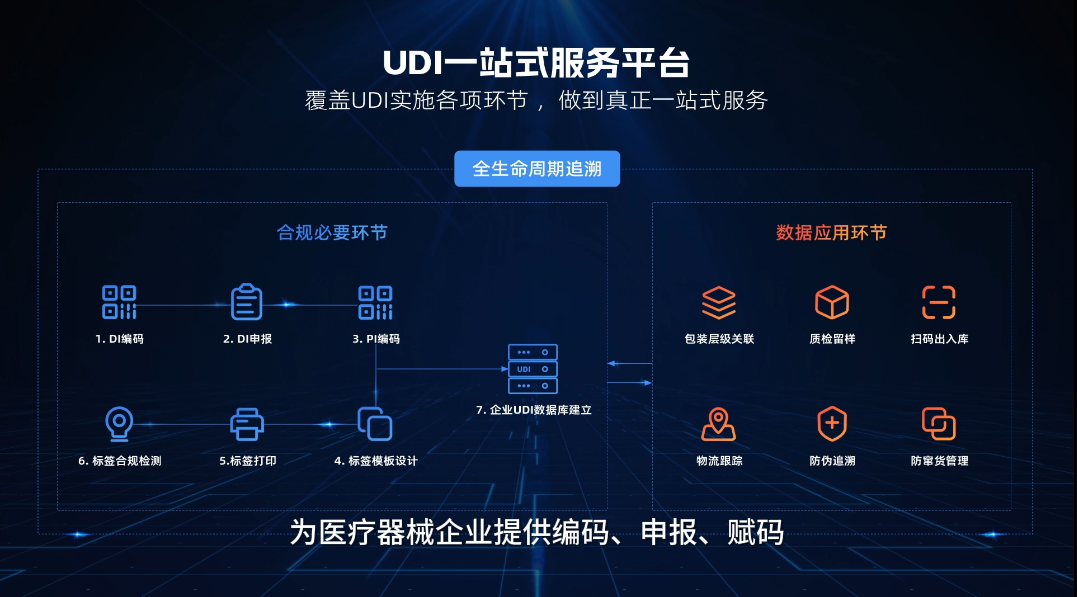
一、【UDI一站式服务平台】:让编码、赋码、追溯变得简单高效
从编码申报、标签赋码,到产线检测、数据上报国家数据库,再到产品追溯,睿展数据的UDI一站式服务平台覆盖了全流程。您无需自行研究GS1规则、不必多方对接系统,也无需担心标签打印出错或数据不同步。该平台已与主流的ERP、MES系统实现对接,可直接嵌入您的生产流程,有效减少人工操作,降低差错率。众多不同规模的企业已借助这套方案顺利通过UDI合规检查。
二、【DMS体系文件管理系统】:让文件管理告别纸质存档,迎检更从容
DMS(体系文件管理系统)可帮助您高效管理质量手册、程序文件、记录表单等所有受控文档。从文件创建、审批、分发、培训,到变更、归档、废止,全部操作在线上完成,全程可追溯。系统内置审计追踪、权限控制、电子签名功能,完全符合新版GMP及FDA 21 CFR Part 11的相关要求。您不再需要担心文件版本混乱、培训记录缺失或检查时翻找资料——所有记录一键调取,迎检轻松有序。

三、睿展数据带给您的核心价值
专业深度:核心团队兼具法规研究、软件研发与UDI一线实施经验,能精准解读政策,提供落地指导。
产品闭环:提供从UDI智能申报与标签管理系统到合规DMS系统的完整产品链,打通质量管理数据孤岛。
服务保障:支持本地化部署、SaaS灵活选用及定制化开发,已助力众多企业通过药监检查与海外注册审核。
新版《医疗器械生产质量管理规范》对UDI和文件管理提出了更高要求,合规不是终点,而是企业提质增效、走向国际市场的起点。
如果您正在为UDI实施或体系文件管理数智化转型而困扰,欢迎联系我们。
睿展数据可为您提供从现状评估、系统部署到验证培训的全流程服务,助您轻松应对监管,加速出海布局。







